El lactato sérico es uno de los biomarcadores pronósticos más sólidos en el contexto de la sepsis. Sin embargo, su interpretación continúa siendo simplificada en muchos entornos clínicos, reduciéndose erróneamente a un marcador de “metabolismo anaerobio por falta de oxígeno”.
En realidad, la hiperlactatemia en la sepsis es el resultado de una alteración compleja entre producción aumentada, disfunción mitocondrial, alteración microcirculatoria y disminución del aclaramiento hepático.
Para la enfermería de urgencias, comprender esta fisiopatología no es un ejercicio académico: es una herramienta clínica de alto impacto en la toma de decisiones.
Metabolismo del lactato: fundamentos bioquímicos
En condiciones fisiológicas:
- La glucosa se metaboliza a través de la glucólisis hasta piruvato.
- El piruvato entra en la mitocondria y se oxida en el ciclo de Krebs.
- Una fracción del piruvato se convierte en lactato mediante la enzima lactato deshidrogenasa (LDH).
El lactato no es un “residuo metabólico”. Es un intermediario dinámico que puede reutilizarse como sustrato energético, especialmente a través del ciclo de Cori (músculo-hígado).
En situaciones normales existe equilibrio entre producción y aclaramiento.
En la sepsis, este equilibrio se rompe.
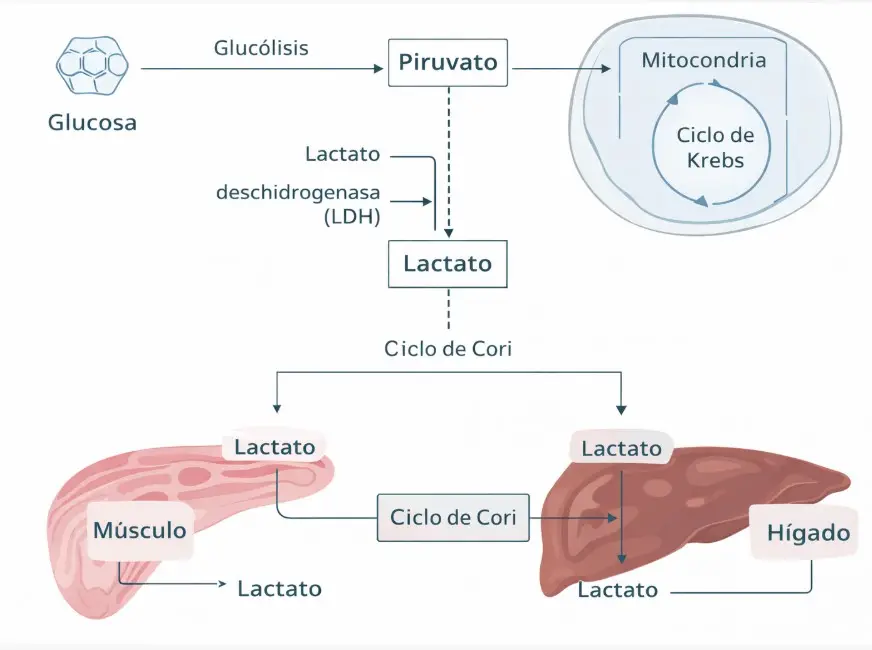
Figura 1. Representación esquemática del metabolismo del lactato y su equilibrio fisiológico entre producción y aclaramiento.
Tipos de hiperlactatemia en sepsis
1. Hiperlactatemia tipo A (hipóxica)
Se produce cuando hay disminución del aporte de oxígeno tisular (DO₂), secundaria a:
- Hipotensión.
- Disminución del gasto cardíaco.
- Hipovolemia.
- Alteración grave de la perfusión.
En este contexto, el metabolismo anaerobio se incrementa como consecuencia directa del descenso crítico del DO₂.
Este es el modelo clásico. Pero no es el único.
2. Hiperlactatemia tipo B (no hipóxica)
Frecuente en sepsis avanzada.
Incluye:
- Disfunción mitocondrial inducida por citocinas inflamatorias.
- Inhibición parcial de la cadena respiratoria.
- Alteración del acoplamiento oxidativo.
- Estimulación β-adrenérgica que acelera la glucólisis aerobia.
En este contexto, puede existir adecuada presión arterial y saturación venosa, pero persistir lactato elevado.
La célula dispone de oxígeno, pero no puede utilizarlo de forma eficaz debido a una disfunción mitocondrial
Este fenómeno explica el llamado “shock oculto”.
Disfunción microcirculatoria: el verdadero núcleo fisiopatológico
En la sepsis, la alteración hemodinámica no se limita a la macrocirculación. El problema central se sitúa en la microcirculación, donde se produce una profunda disrupción estructural y funcional del endotelio.
En este contexto ocurre:
- Activación endotelial masiva mediada por citocinas proinflamatorias.
- Pérdida del glucocálix vascular, con alteración de la barrera endotelial.
- Aumento de la permeabilidad capilar y fuga plasmática.
- Formación de microtrombos por activación de la coagulación intravascular.
- Aparición de shunts microvasculares con flujo no nutritivo.
El resultado no es una simple disminución global del flujo, sino una distribución heterogénea del mismo. Algunas áreas tisulares reciben perfusión adecuada, mientras otras permanecen críticamente hipoperfundidas.
Este fenómeno genera desacoplamiento entre:
- Presión arterial sistémica.
- Flujo macrohemodinámico.
- Perfusión celular efectiva.
Puede existir tensión arterial aparentemente conservada mientras determinados territorios tisulares presentan hipoxia celular y metabolismo anaerobio.
La macrocirculación puede parecer estable.
La microcirculación no lo está.
Este desacoplamiento explica el llamado shock compensado o shock oculto, en el que:
Paciente normotenso + lactato ≥2 mmol/L
= probable hipoperfusión microcirculatoria significativa.
Desde la práctica enfermera avanzada en urgencias, este concepto es esencial. Permite comprender por qué un paciente “estable” puede deteriorarse rápidamente si no se actúa sobre la disfunción perfusional subyacente.
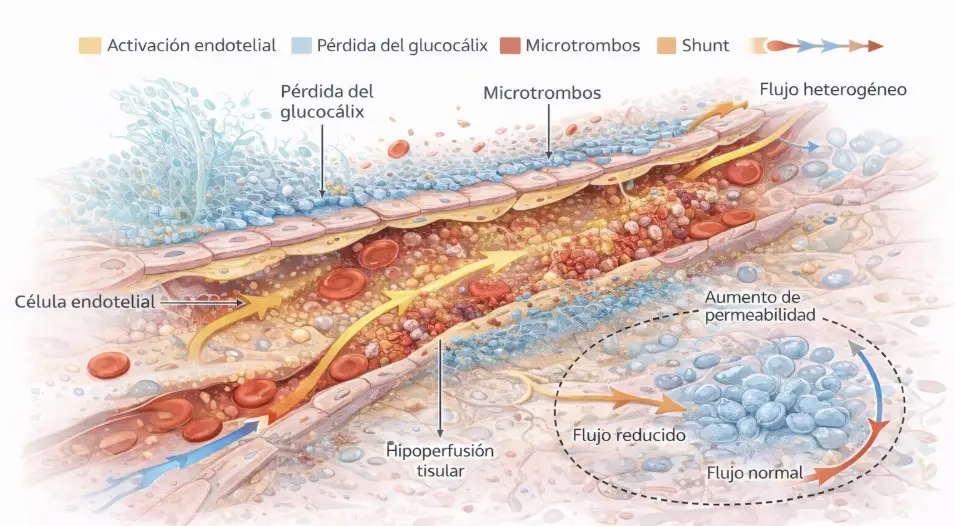
Figura 2. Representación esquemática de la disfunción microvascular en la sepsis con pérdida del glucocálix, formación de microtrombos y heterogeneidad del flujo.F
DO₂, VO₂ y deuda de oxígeno en la sepsis
En condiciones fisiológicas, el consumo tisular de oxígeno (VO₂) se mantiene estable aunque el aporte sistémico (DO₂) disminuya de forma moderada. Esto es posible gracias al aumento compensatorio de la extracción de oxígeno por parte de los tejidos.
Mientras el DO₂ permanece por encima de un umbral crítico, el metabolismo celular continúa siendo predominantemente aeróbico.
Sin embargo, cuando el aporte de oxígeno cae por debajo de ese punto crítico —ya sea por disminución del gasto cardíaco, hipovolemia, anemia o alteración microvascular— el consumo de oxígeno pasa a depender directamente del aporte disponible.
En ese momento comienza a desarrollarse metabolismo anaerobio y aparece la denominada deuda de oxígeno.
La deuda de oxígeno representa el desequilibrio entre las necesidades metabólicas celulares y la capacidad real de generar energía mediante fosforilación oxidativa. Cuanto mayor es su magnitud y más tiempo persiste, mayor es el riesgo de disfunción orgánica.
En la sepsis, este fenómeno no siempre responde únicamente a una caída global del DO₂. Puede existir un aporte aparentemente adecuado, pero con alteración en la distribución microvascular o disfunción mitocondrial que impide una utilización eficiente del oxígeno.
En este contexto, la hiperlactatemia actúa como marcador indirecto de desequilibrio metabólico y posible acumulación de deuda energética.
Desde la práctica enfermera en urgencias, comprender este modelo permite interpretar el lactato como expresión de fracaso perfusional dinámico y no como una cifra aislada. La identificación precoz y la corrección rápida de la hipoperfusión son determinantes para limitar la progresión hacia el shock séptico.
🔒 Contenido exclusivo para socios SEEUE
Este contenido avanzado sobre fisiopatología hemodinámica en la sepsis está disponible exclusivamente para socios activos de SEEUE
La pertenencia a la sociedad permite acceder a contenidos científicos ampliados, recursos clínicos y formación especializada en urgencias y emergencias.
¿Ya eres socio? Inicia sesión.
Valor pronóstico del lactato en urgencias
La elevación del lactato en el contexto de sospecha de sepsis se asocia de forma consistente con mayor riesgo de deterioro clínico y mortalidad.
Diversos estudios han demostrado que:
- Lactato ≥2 mmol/L ya se correlaciona con aumento de riesgo.
- Lactato ≥4 mmol/L se asocia a mayor probabilidad de shock séptico y fracaso multiorgánico.
- La persistencia de hiperlactatemia tras reanimación inicial es un marcador de mal pronóstico.
Sin embargo, la interpretación del lactato no debe realizarse de forma aislada. Su valor clínico depende de la integración con:
- Estado hemodinámico.
- Signos de hipoperfusión.
- Evolución temporal.
- Respuesta al tratamiento.
En urgencias, un paciente normotenso con lactato elevado puede encontrarse en una fase precoz de disfunción perfusional. Identificar esta situación permite anticipar deterioro antes de que aparezca hipotensión franca.
Por ello, el lactato no debe entenderse únicamente como marcador de gravedad, sino como herramienta dinámica de monitorización.
El valor absoluto inicial es relevante, pero la tendencia evolutiva es determinante.
Clearance de lactato y respuesta a la reanimación
El concepto de lactate clearance hace referencia a la reducción porcentual del lactato tras el inicio del tratamiento.
Más que un valor aislado, lo que interesa en urgencias es la evolución en las primeras horas.
De forma práctica:
- Una disminución significativa del lactato en las primeras 2–6 horas se asocia con mejor pronóstico.
- La persistencia o aumento del lactato sugiere hipoperfusión mantenida o fracaso en la respuesta terapéutica.
El clearance puede calcularse de forma sencilla:
Clearance (%) =(Lactato inicial − Lactato a 2–4 h) ÷ Lactato inicial × 100
Aunque no siempre se calcula formalmente en urgencias, la comparación seriada permite evaluar la eficacia de:
- Expansión con fluidos.
- Optimización hemodinámica.
- Control del foco infeccioso.
- Inicio precoz de antibioterapia.
Es importante recordar que la normalización del lactato no siempre es inmediata. En algunos pacientes puede persistir elevación moderada pese a estabilidad hemodinámica, especialmente si existe disfunción mitocondrial o alteración hepática en el aclaramiento.
Por ello, la interpretación debe integrarse con la evolución clínica global.
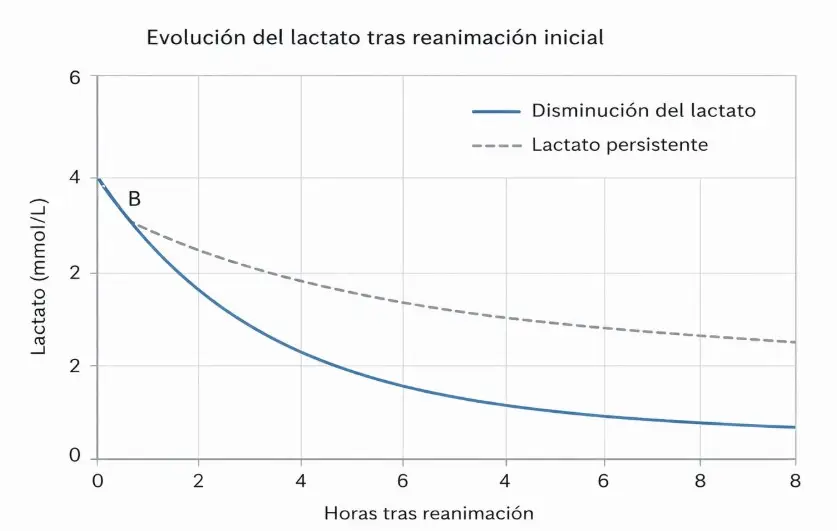
Figura 3. Ejemplo esquemático de evolución del lactato en las primeras horas tras la reanimación inicial en sepsis.
Errores frecuentes en la interpretación del lactato en urgencias
A pesar de su utilidad, el lactato sigue siendo interpretado de forma simplista en muchos entornos asistenciales. Algunos errores frecuentes incluyen:
1. Considerarlo únicamente un marcador de hipotensión.
La hiperlactatemia puede estar presente en pacientes normotensos con disfunción microcirculatoria. Esperar a la caída de la presión arterial retrasa la intervención.
2. No repetir la determinación.
El valor aislado tiene menor relevancia que su evolución en las primeras horas. La ausencia de control seriado limita la capacidad de monitorización.
3. Atribuir su elevación exclusivamente a causas benignas.
Ejercicio previo, ansiedad o dolor pueden elevar el lactato, pero en contexto de sospecha infecciosa debe priorizarse siempre la hipótesis de hipoperfusión hasta demostrar lo contrario.
4. Interpretarlo sin integrar el contexto clínico.
El lactato debe correlacionarse con relleno capilar, diuresis, estado mental, frecuencia respiratoria y respuesta hemodinámica.
5. Buscar la normalización inmediata.
La reducción progresiva es más relevante que la normalización absoluta en las primeras horas.
Conclusión
El lactato en la sepsis no es un simple marcador bioquímico. Es la expresión metabólica de un desequilibrio perfusional que puede preceder al deterioro hemodinámico evidente.
Su correcta interpretación exige comprender la fisiopatología subyacente, integrar el contexto clínico y valorar su evolución en las primeras horas de tratamiento.
En urgencias, la determinación precoz y la monitorización seriada del lactato permiten identificar hipoperfusión oculta, anticipar progresión a shock séptico y evaluar la respuesta a la reanimación inicial.
Más que una cifra aislada, el lactato debe entenderse como una herramienta dinámica de evaluación clínica.
Desde la práctica enfermera avanzada, su análisis riguroso refuerza la capacidad de toma de decisiones y contribuye a una atención más precoz, precisa y segura del paciente séptico.
🔎 Amplía este contenido
Si quieres profundizar en la activación precoz y el manejo protocolizado del paciente séptico en urgencias, consulta nuestro artículo:
Para profundizar en la valoración y manejo integral del paciente séptico en urgencias, consulta también:
👉 Código Sepsis en urgencias: activación paso a paso para enfermería
👉 qSOFA en urgencias: cuándo usarlo y cuándo no
👉 Sepsis en urgencias: actuación de enfermería paso a paso